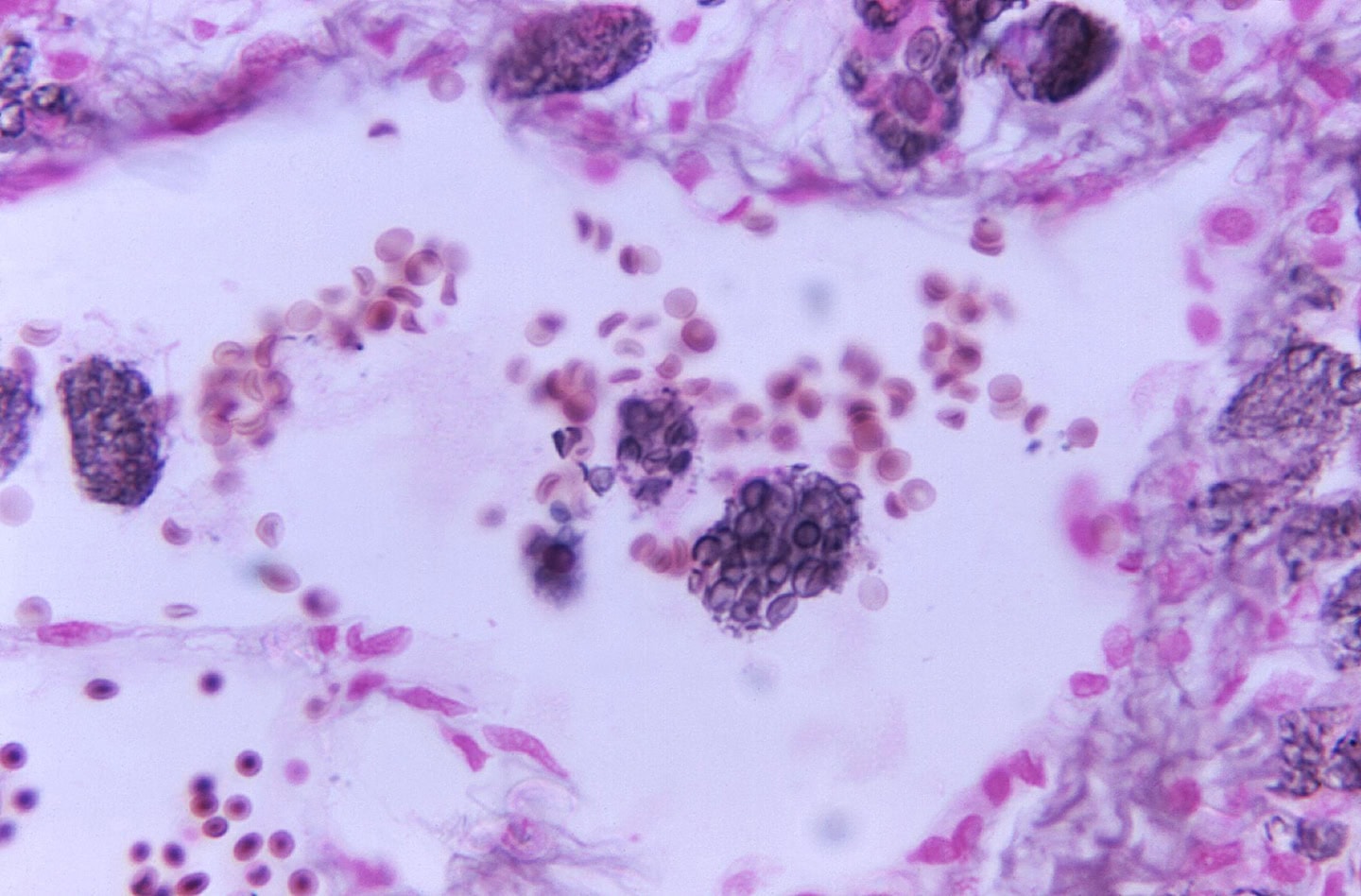
Combater infecções bacterianas e virais está se tornando cada vez mais difícil devido à crescente resistência desses microrganismos aos medicamentos. Já não se pode contar apenas com os antibióticos para vencer bactérias perigosas. E os antivirais nem sempre conseguem derrotar os vírus. Esse é um problema enorme, mas que já é amplamente reconhecido e pesquisado.
Existe, no entanto, um desafio médico adicional — e de grande importância: os fungos resistentes a medicamentos.
Sim, fungos.
É um tema pouco discutido — e isso preocupa Paul Verweij, professor de micologia clínica no Centro Médico da Universidade Radboud, em Nijmegen, na Holanda. Ele afirma que há um “aumento silencioso” de fungos resistentes a medicamentos e que esse fenômeno está ocorrendo, em grande parte, de forma despercebida.
Esse desafio é particularmente acentuado em países de baixa renda.
“Veja, por exemplo, a *Candida auris* [um tipo de levedura que pode causar infecções graves e é frequentemente resistente a medicamentos]: são necessárias medidas de controle de infecção extremamente rigorosas nos hospitais; é preciso ter bons diagnósticos e um controle de infecção eficaz; é preciso fazer o acompanhamento dos pacientes — e nada disso está disponível nesses países de baixa e média renda”, diz ele. “As pessoas vão morrer sem que se saiba que elas tinham uma infecção fúngica. Não haveria como saber se essa infecção era resistente.”
Verweij uniu forças com 50 cientistas de diversas partes do mundo — do Brasil à Nigéria, passando pela China — para, nesta semana, publicar na revista *Nature Medicine* um apelo por ações de combate aos fungos resistentes a medicamentos.
A NPR conversou com Verweij, que atua nessa área há mais de 20 anos. A entrevista foi editada para fins de clareza e concisão.
Qual é a relação entre a agricultura e os fungos resistentes a medicamentos?
Os fungicidas são utilizados para proteger as plantas contra doenças causadas por fungos. Praticamente tudo — melancias, milho, trigo, flores — requer o uso intensivo de fungicidas. Se não utilizássemos esses fungicidas, provavelmente teríamos uma perda de produtividade da ordem de 30% a 40%.
O problema é que os fungicidas são bastante semelhantes aos medicamentos que administramos aos pacientes. Assim, o fungo torna-se resistente ao fungicida e, ao mesmo tempo, nossos azóis médicos [uma classe de medicamentos antifúngicos] já não funcionam tão bem.
Os fungos que causam doenças em humanos não são os mesmos que causam doenças nas plantas. Portanto, este é um efeito não intencional.
Como a resistência se propaga das fazendas para os hospitais?
Os bolores — aqueles fungos de aspecto filamentoso — possuem esporos que são liberados no ar. Esses esporos percorrem longas distâncias. O mecanismo não é totalmente compreendido, mas a hipótese é que eles ascendam até as correntes de jato — a grandes altitudes na atmosfera — e, a partir daí, possam viajar por continentes inteiros. Nós inalamos esses esporos o tempo todo.
Quão graves são as infecções fúngicas?
No caso dos fungos, existem dois tipos de infecções. Primeiro, temos as infecções muito graves; estas geralmente ocorrem em pacientes [hospitalizados] que apresentam algum tipo de deficiência imunológica — por exemplo, leveduras na corrente sanguínea ou bolores nos pulmões. Segundo, temos as infecções da pele, do cabelo e das unhas, que são irritantes, mas não representam risco de vida.
Nos últimos 10 a 20 anos, temos observado uma resistência cada vez maior nos fungos de ambas as categorias.
Existem pouquíssimos estudos que avaliem o impacto clínico dessa resistência. Realizamos um estudo na Holanda e constatamos que, ao comparar uma infecção [na qual os antifúngicos azólicos são eficazes] com uma infecção resistente, observa-se uma diferença de cerca de 20% na taxa de mortalidade — ou seja, a probabilidade de óbito aumenta em 20%. Trata-se, portanto, de um impacto significativo. Além disso, surgiu uma nova doença de pele [causada pelo *Trichophyton indotineae*] que, embora não resulte em óbito, já afetou pacientes que estão em tratamento há quatro anos e continuam sofrendo com a infecção.
Por que é tão difícil desenvolver novos medicamentos antifúngicos?
O principal desafio reside no fato de que os fungos — se observarmos sua estrutura celular, ou seja, sua constituição interna — são muito semelhantes às células humanas. Isso difere do que ocorre com as bactérias, pois estas possuem uma estrutura muito mais simples. Já os vírus são ainda mais simples, uma vez que sequer possuem uma estrutura celular propriamente dita.
No caso dos fungos — justamente por serem semelhantes às células humanas —, torna-se bastante difícil encontrar um medicamento capaz de eliminar o fungo sem, ao mesmo tempo, causar danos às células do organismo humano. Assim, nos últimos 75 anos, desenvolvemos apenas cinco classes de antifúngicos. Os azóis são, de longe, os mais importantes.
O problema é que, se você não puder utilizar uma dessas classes, talvez lhe reste apenas uma alternativa. Isso já está causando problemas. Por exemplo, se o fungo estiver no cérebro, há pouquíssimos medicamentos que de fato conseguem penetrar nesse órgão.
O que pode ser feito?
Em um congresso de micologia, encontramos uma comunidade global disposta a colaborar [nesta questão].
Por exemplo, é fundamental saber o que as pessoas estão utilizando [nas lavouras] e verificar se é possível reduzir esse uso ou se há alguma aplicação desnecessária. Outro fator importante é: caso novos fungicidas sejam introduzidos, eles [devem] passar por uma avaliação para determinar seu impacto sobre os patógenos fúngicos humanos. É essencial estabelecer se existe risco de resistência cruzada.
Você está otimista?
Trabalho nesta área há muito tempo e acredito que ela está mudando.
A OMS publicou, pela primeira vez em 2022, uma lista de patógenos fúngicos — o que teve um grande impacto. Há uma década, quando a Organização Mundial da Saúde lançou seu plano de ação global contra a resistência antimicrobiana, os fungos foram mencionados apenas duas vezes. Agora, passados 10 anos, esse plano está sendo revisado. E, como comunidade micológica, sentimos que é realmente importante, neste momento, que os fungos sejam devidamente abordados.
O problema é que, no que diz respeito aos fungos, precisamos realizar o trabalho básico: desenvolver as ferramentas, realizar a vigilância e estabelecer as redes [laboratoriais]. E, por vezes, é difícil conseguir financiamento para essas ações fundamentais.
Mas, no geral, acredito que o cenário está realmente mudando. As pessoas estão percebendo que este não é um problema local — é, de fato, global.
Fonte: npr.org